
Neurotoxiciteit is een bekende bijwerking van CAR T-celtherapie in de acute fase. In een Franse studie werd gekeken naar mogelijke neurologische langetermijneffecten van de therapie. Voorafgaand aan CAR T-celtherapie en 2 jaar na behandeling werden lymfoompatiënten onderzocht met behulp van neurologisch onderzoek, neuropsychologische tests, MRI en diverse vragenlijsten. De onderzoekers vonden geen verschillen voor en na behandeling. Tijdens EAN presenteerde dr. Renata Ursu (Université de Paris-Cité, Frankrijk) de resultaten van deze prospectieve studie.
Voor een toenemend aantal aandoeningen wordt chimeer-antigeenreceptor(CAR) T-celtherapie ingezet. Met name bij hematologische maligniteiten heeft CAR T-celtherapie positieve resultaten laten zien. De behandeling gaat echter gepaard met ernstige bijwerkingen. Cytokine release syndroom (CRS) is de meest voorkomende bijwerking van CAR T-celtherapie. Daarnaast is neurotoxiciteit, ook wel immuun-effectorcel-geassocieerd neurotoxiciteitssyndroom (ICANS) genoemd, een veelvoorkomende bijwerking van CAR T-celtherapie. Een meta-analyse van 12 klinische studies met meer dan 800 patiënten behandeld met anti-CD19 CAR T-cellen bij B-celmaligniteiten toonde neurotoxiciteit van enige graad bij circa 50% van de patiënten en graad 3/4 bij circa 20%. De pathofysiologie van ICANS is nog niet helemaal begrepen, maar treed over het algemeen iets later op dan CRS en heeft een mediane duur van 6 dagen. Het overgrote deel van de patiënten herstelt binnen één maand na de CAR T-celinfusie. Over eventuele neurotoxiciteit van CAR T-celtherapie op de lange termijn is niets bekend.
Om dit te onderzoeken werden in de periode tussen 1 juli 2018 en 30 augustus 2019 patiënten met CAR T-celtherapie voor lymfoom prospectief gevolgd. Patiënten werden voorafgaand aan de CAR T-celtherapie neurologisch geëvalueerd, kregen een MRI van de hersenen, neuropsychologische tests en een aantal vragenlijsten. Patiënten die na 2 jaar geen tumorprogressie lieten zien, werden op dat moment opnieuw neurologisch onderzocht.
In totaal deden 52 patiënten mee aan de neurologische evaluatie voorafgaand aan de CAR T-celtherapie. Hiervan waren na 2 jaar 19 patiënten in leven zonder progressie van het lymfoom. Mediane leeftijd was 69 jaar en 9 patiënten waren vrouw. Van acute neurotoxiciteit was sprake bij 11 van de 19 patiënten; 8 met graad 1/2, en 3 met graad 3/4. Bij 8 van de 11 was dit in de vorm van een cognitieve stoornis. Alle 11 patiënten herstelden binnen 42 dagen.
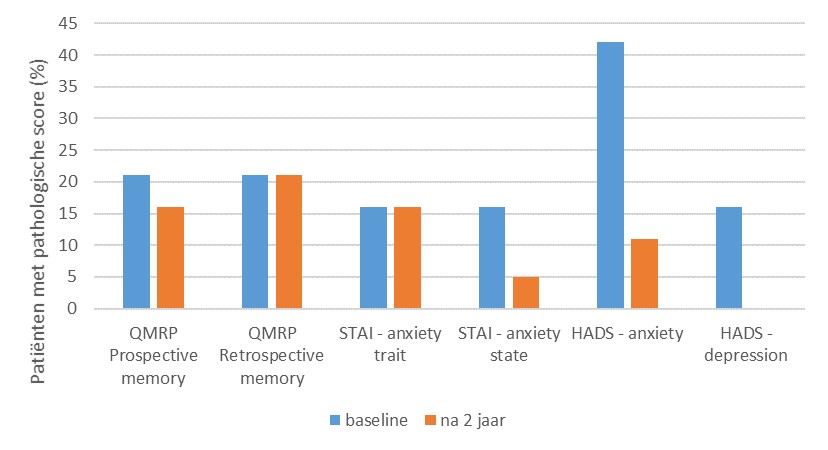
Na 2 jaar was het neurologisch onderzoek vergelijkbaar bij alle patiënten. Eén 44-jarige patiënt zonder acute neurotoxiciteit gaf aan dat hij last had van een milde en fluctuerende paresthesie. Bloed- en CSF-waarden waren bij deze patiënt echter normaal, evenals de MRI en EMG. Bij geen van de patiënten werden na 2 jaar verschillen gevonden op MRI. Ook ten aanzien van de uitgebreide neuropsychologische tests 2 jaar na de CAR T-celtherapie werd geen verschil gevonden. Dat gold ook niet voor de subgroep van patiënten met eerdere acute neurotoxiciteit. De vragenlijsten gingen over angst, depressie en cognitieve klachten. Er werd geen verschil tussen baseline en na 2 jaar gevonden voor geheugen (zie Figuur 1). Wel was dit het geval voor angst en depressie. De onderzoekers schrijven dit toe aan de verbeterde vooruitzichten van patiënten ten aanzien van het B-cellymfoom.
De onderzoekers zagen in deze prospectieve studie geen neurologische gevolgen op de lange termijn volgend na CAR T-celtherapie. De behandeling was niet geassocieerd met cognitieve achteruitgang en MRI-afwijkingen. Voor meer robuuste conclusies zijn echter studies nodig met grotere aantallen en ook met verschillende typen CAR T-celtherapie.
Referentie
Ursu R, et al. Long term neurological safety in B-cell lymphoma patients treated with CAR T-cell therapy: a prospective cohort study. Gepresenteerd tijdens EAN 2022; abstract OPR-154.