

Het Rett-syndroom (RTT) is een ernstige invaliderende neurologische ontwikkelingsstoornis waarvoor nog geen goedgekeurde behandeling bestaat. In de meeste gevallen wordt RTT veroorzaakt door een mutatie van het MECP2-gen dat codeert voor een DNA-bindend eiwit dat in hoge concentraties in het zenuwstelsel voorkomt. In de LAVENDER fase III-studie werd na 12 weken behandeling met trofinetide een significant betere werkzaamheid aangetoond ten opzichte van placebo. Resultaten werden tijdens AAN 2022 gepresenteerd door Jeffrey Neul, MD, PhD van het Vanderbilt Kennedy Center (Nashville, Verenigde Staten).
Na een ogenschijnlijk normale ontwikkeling vanaf de geboorte beginnen RTT-patiënten bij 6 tot 18 maanden een vertraging in de ontwikkeling van hun vaardigheden te vertonen. De aandoening treft voornamelijk meisjes en vrouwen met een frequentie van ongeveer één op de 10.000-15.000. Na 18 tot 30 maanden treedt regressie op en verliezen patiënten met name de verworven doelgerichte handvaardigheid en de gesproken taal. Bovendien ontwikkelen ze een karakteristieke repetitieve handbeweging en het onvermogen om te lopen. Daarnaast komen ook epileptische aanvallen en (ernstige) constipatie voor. Trofinetide is een nieuw synthetisch analoog van glycine-proline-glutamaat (GPE) dat is afgeleid van de insuline-achtige groeifactor 1. Aan proline is een methylgroep toegevoegd dat de kwaliteit van het middel verbetert, het oraal werkzaam maakt en het een langere halfwaarde geeft waardoor het tweemaal per dag kan worden toegediend.
In deze dubbelblinde, gerandomiseerde, placebogecontroleerde fase III-studie (LAVENDER) ontvingen 187 vrouwen met RTT in de leeftijd van 5-20 jaar trofinetide of placebo gedurende een behandeling van 12 weken. Patiënten ontvingen een op het gewicht afgestemde dosering. De primaire eindpunten waren de uitkomsten van de ‘Rett Syndrome Behaviour Questionnaire’ (RSBQ) en de ‘Clinical Global Impression of Improvement Scale’ (CGI-I). De RSBQ is een vragenlijst voor zorgverleners die met 45 onderdelen een breed spectrum beslaat van de klinische kenmerken en symptomen die bij RTT voorkomen. De CGI-I is een schaal met 7 onderdelen van specifieke RTT-kenmerken waarmee behandelend artsen beoordelen hoeveel een patiënt is verbeterd of verslechterd in een bepaalde periode. Het secundaire eindpunt was een beoordeling door zorgverleners op basis van 13 aspecten van communicatie en prelinguistische vaardigheden volgens een schaal die voorheen werd gebruikt bij neurologische ontwikkelingsaandoeningen zoals RTT (CSBS-DP-IT Social).
De studie liet voor beide primaire eindpunten een significant voordeel zien van trofinetide ten opzichte van placebo met een middelmatig effect volgens beoordeling van de Cohen’s d effectgrootte (bij RSBQ: 0,37 [p=0,0175] en bij CGI-I: 0,47 [p=0,003], zie Figuur 1).
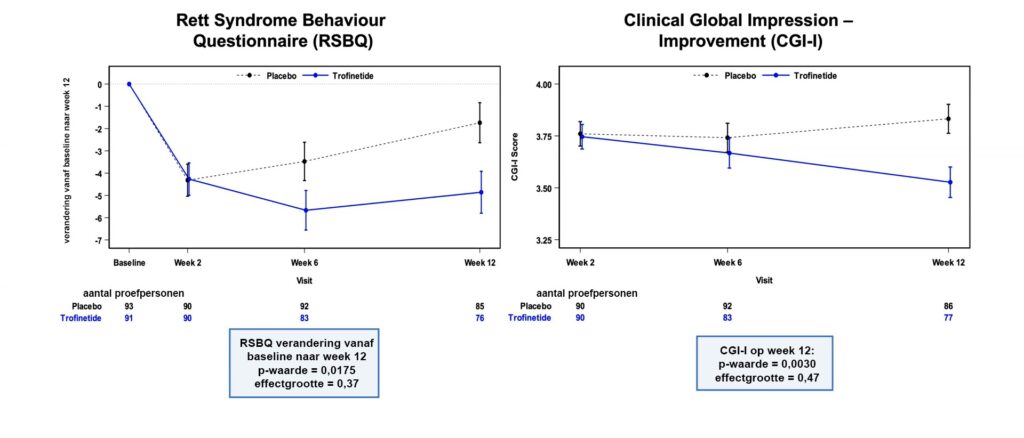
Dat gold eveneens voor het secundaire eindpunt van de samengestelde sociale schaal (CSBS-DP-IT Social: 0,43 [p=0,0064]). Behandelingsgerelateerde bijwerkingen (TEAE’s) van alle graden werden gezien bij 92,5% van de patiënten in de trofinetide-groep en 54% in de placebogroep. Er waren geen verschillen in ernstige TEAE’s tussen beide groepen (beide 3,2%). Bij 17% van de patiënten in de trofinetide-groep leidden TEAE’s tot het staken van de behandeling vergeleken met 2% in de placebogroep. De meest voorkomende TEAE’s in de trofinetide-groep waren diarree (80% vs. 18%) en braken (24% vs. 9%). In de meeste gevallen waren de bijwerkingen mild tot matig van aard.
Ten aanzien van klinische kenmerken communicatieve vaardigheden gaf 12 weken behandeling met trofinetide een significante verbetering ten opzichte van placebo bij patiënten met RTT. Deze voordelen waren onafhankelijk van de leeftijd of de ernst van de ziekte en traden gelijkelijk op in alle onderzochte subgroepen. Er was sprake van een acceptabel veiligheidsprofiel van trofinetide, waarbij diarree en braken het vaakst voorkwamen. In de meeste gevallen waren deze mild tot matig van aard.
Referentie
Neul JF, Percy AK, Benke TA, et al. Efficacy and Safety of Trofinetide for the treatment of Rett Syndrome: Results from the Phase 3 LAVENDER Study. Gepresenteerd tijdens AAN virtual 2022, op 25 april 2022.